Perkembangan Teori Atom
Nah kayak yang udah dijanjikan sebelumnya kita bakal bahas perkembangan teori atom.
kalian perlu tau dulu dari dari kata 'Atom' itu sendiri.
Zaman dahulu saat abad ke-4 sebelum masehi diperkirakan ada seorang fisul dari yunani , Democritus. Ia mengemukakan sebuah teori bahwa setiap benda dapat dibelah-belah hingga menjadi bagian paling kecil yang tidak dapat dibagi lagi.
Materi yang tidak dapat dibelah lagi itu disebut Atom. Atom sendiri berasal dari kata A dan TOMos yang berarti 'tidak' dan 'dipotong-potong'. Tapi pada saat itu belum ada teori tentang atom seperti sekarang.
Kita bakal masuk ke 5 Perkembangan Teori Atom
Teori Atom Dalton
Teori atom Dalton ditemukan oleh John Dalton dan merupakan teori atom pertama yang dilandasi data ilmiah. Pokok-pokok teori atom Dalton adalah sebagai berikut:
- Atom merupakan partikel zat atau materi terkecil yang tidak dapat dibagi lagi menjadi bagian yang lebih kecil.
- Atom berbentuk/digambarkan seperti bola sederhana yang berukuran sangat kecil.
- Suatu unsur tersusun dari atom-atom yang sama, sedangkan senyawa tersusun dari atom-atom yang berbeda sesuai unsur penyusunnya.
- Atom-atom bergabung membentuk senyawa dengan perbandingan bilangan bulat dan sederhana.
- Reaksi kimia merupakan pemisahan, penggabungan, atau penyusunan kembali atom-atom sehingga atom tidak dapat diciptakan atau dimusnahkan.
Teori Atom Thomson
J.J. Thomson menggambarkan model atomnya setelah dia menemukan sinar katode. Dia menyimpulkan bahwa atom adalah bola padat bermuatan positif dan di dalamnya tersebar elektron yang bermuatan negatif. Model atom Thomson seperti kismis(elektron) yang melekat pada roti(atom).
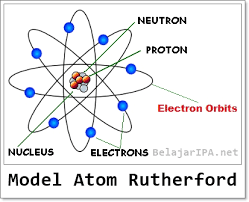
Teori Atom Rutherford
Teori atom Rutherford muncul berdasarkan eksperimen hamburan sinar alfa dari uranium. Kesimpulannya adalah atom terdiri dari inti atom yang sangat kecil dan bermuatan positif, dikelilingi oleh elektron yang bermuatan negatif seperti tata surya. Kelemahan dari model atom Rutherford adalah teori ini tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom.
Teori Atom Bohr
Niels Bohr, melakukan percobaan spektrum hidrogen untuk memperbaiki teori atom Rutherford. Hasil percobaan Bohr adalah elektron-elektron mengelilingi inti atom yang terdiri dari Proton dan Neutron pada lintasan-lintasan tertentu yang disebut kulit elektron atau tingkat energi.
Teori Atom Modern ( Mekanika Kuantum )
Model atom modern ditemukan oleh Schrodinger. Penjelasan model atom modern adalah elektron-elektron yang mengelilingi inti atom memiliki tingkat energi tertentu tetapi keberadaannya tidak dapat dipastikan. Elektron berada di dalam orbital-orbital yang merupakan fungsi gelombang tertentu dalam kulit atom yang disebut sebagai daerah dengan kebolehjadian paling besar untuk menemukan elektron. Model atom modern disebut juga model atom Schrodinger.
Nah untuk sekarang segini dulu ya bakalan diUpdate kok biar lebih lengkap disetiap hal yang bakal kita fokusin